- I) Organisation et composition du système nerveux
- 1) Organisation du système nerveux
- 2) Le neurone
- a) Morphologie du neurone
- b) La gaine de myéline
- c) Classification des neurones
- 3) Névroglie : cellules gliales et cellules de Schwann
- II) Transmission de l’influx nerveux et synapses
- 1) Potentiels et influx nerveux
- a) Le potentiel de repos
- b) Le potentiel gradué
- c) Le potentiel d’action
- 2) Synapses et neurotransmissions
- 1) Potentiels et influx nerveux
- III) Encéphale, moelle épinière et nerfs rachidiens
- 1) L’encéphale
- 2) La moelle épinière et les nerfs rachidiens
- a) Substance grise et racine des nerfs rachidiens
- b) Substance blanche
- IV) Le réflexe
- V) Le système nerveux autonome (SNA)
- 1) Système nerveux sympathique (ou orthosympathique)
- 2) Système nerveux parasympathique (ou vagal)
I) Organisation et composition du système nerveux
Le système nerveux et le système endocrinien permettent le maintient de l’homéostasie. Le système endocrinien sécrète des hormones dans le sang, leurs actions est lente mais soutenue dans le temps (cf. cours sur l’endocrinologie). Le système nerveux quant à lui permet la formation d’influx nerveux qui ont une action rapide mais brève, on parle ici de neuromédiateurs qui agissent sur de très courte distance (quelques µm) au niveau des synapses.
Le système nerveux est divisé en deux grandes zones : le système nerveux central (SNC) et le système nerveux périphérique (SNP). Le système nerveux central est constitué de l’encéphale (cerveau) et de la moelle épinière, et le système nerveux périphérique est constitué des ganglions nerveux et des nerfs : 12 paires de nerfs crâniens et 31 paires de nerfs rachidiens.
Le système nerveux a 3 fonctions essentielles :
- Une fonction sensitive de détection grâce à des récepteurs qui détectent toutes les modifications de l’organisme et l’environnement extérieur.
- Une fonction d’intégration et d’analyse des informations qu’il reçoit des récepteurs.
- Une fonction motrice permettant la contraction des diverses cellules musculaires de l’organisme.
1) Organisation du système nerveux
Toutes les informations de l’organisme affluent vers le SNC à partir de détecteurs sensoriels de différents types.
Le SNP est constitué de deux voies :
- La voie sensitive (voie afférente) constituée de neurones sensitifs somatiques et viscéraux, et au niveau de laquelle la propagation des influx vient des récepteurs périphériques.
- La voie motrice (voie efférente) constituée de neurones moteurs dont l’origine des influx est le SNC. Cette voie motrice peut elle-même être divisée en deux types de système nerveux :
- Le système nerveux autonome (SNA), ou système nerveux végétatif (SNV), est involontaire. L’influx nerveux provenant du SNC est envoyé vers les muscles lisses, le myocarde et les glandes. Il possède le système sympathique (Σ) qui tend à activer les organes et le système parasympathique (pΣ) qui tend à les mettre au repos. Attention, les deux peuvent pourtant être excitateur et inhibiteur.
- Le système nerveux somatique (SNS) est volontaire et l’influx nerveux provenant du SNC est envoyé vers les muscles striés squelettiques.
2) Le neurone
Les cellules nerveuses (neurones) sont les unités fonctionnelles du SNC et forment un réseau qui s’étend dans tout l’organisme. Bien qu’elles ne soient pas les plus nombreuses dans le système nerveux, ce sont les plus importantes. Pour indication le système nerveux possède 10% de neurones pour 90% de cellules gliales (leur rôle dans le système nerveux sera énoncé dans la suite du cours).
Ce sont des cellules post-mitotique (pour la majorité, étant hautement spécialisés) et excitable. En effet on sait aujourd’hui que certains neurones peuvent être produits au niveau de l’hippocampe. Leur excitabilité est due à un changement d’état très rapide qui est déterminé par un facteur extérieur. Les cellules nerveuses peuvent modifier leur anatomie et possèdent une grande longévité. Elles sont très sensibles à l’hypoglycémie et à l’hypoxie. En effet elles consomment presque exclusivement du glucose qui leurs est fournit par les cellules gliales. Les neurones sont indépendants les uns des autres, n’établissant que des contacts fonctionnels spécifiques appelés synapses. Ce sont également des cellules sécrétrices particulières qui peuvent avoir comme produit de sécrétion des neuromédiateurs, des neuromodulateurs ainsi que des neurohormones (GnRH).
Les neurones étant des cellules post-mitotique, elles ne peuvent pas être source de tumeur. Ainsi les tumeurs neuronales n’existent pas, mais attention les tumeurs cérébrales existent (cellules gliales).
a) Morphologie du neurone
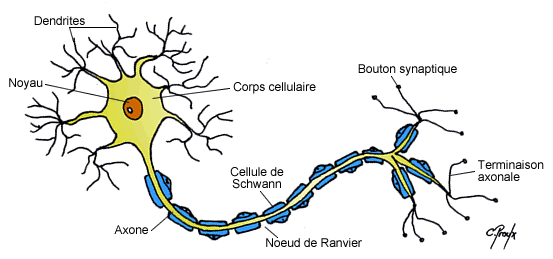
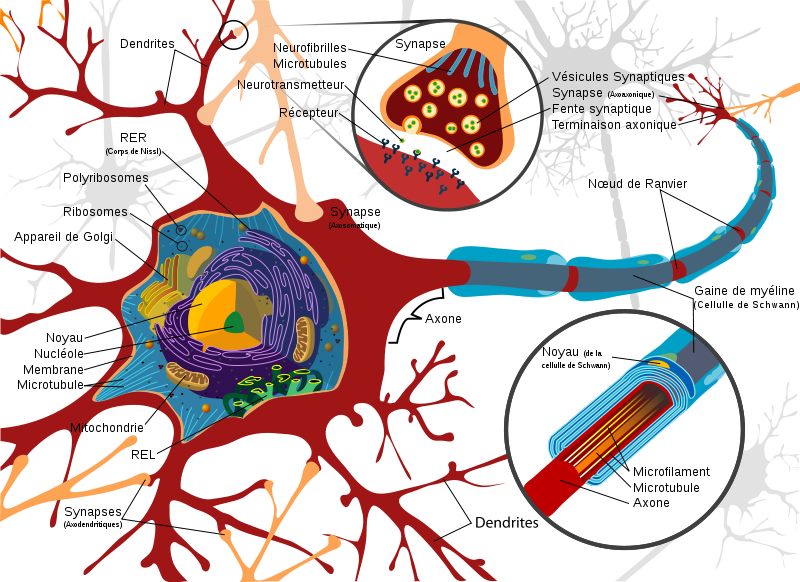
La morphologie du neurone est caractérisée par différentes structures :
- Le corps cellulaire (ou soma ou péricaryon) : est la partie vitale de la cellule. Il est constitué d’un noyau qui détermine la forme du corps cellulaire, le cytoplasme y étant presque accolé, et dont le nucléole est volumineux reflétant ainsi la forte activité de synthèse de ces cellules. Le corps cellulaire est la portion centrale du neurone d’où émergent l’axone et les dendrites. Il possède les mêmes organites que dans la majorité des cellules ; on note cependant la présence d’amas de réticulum endoplasmique granuleux (lieu de synthèse protéique) que l’on appelle corps de Nissl, ainsi qu’une grande quantité de protéines du cytosquelette, appelées neurofibrilles, qui sont responsables de la communication intracellulaire. Un des rôles principaux du corps cellulaire est de synthétiser une grande partie des constituants nécessaires à la structure et aux fonctions du neurone.
- Les dendrites : sont des prolongements fins du péricaryon qui sont présentent en grand nombre. Elles se divisent en multiples branches dont le diamètre est variable tout au long d’une branche et qui peut être plus important que pour l’axone. L’arborisation formée par les dendrites est spécifique du type de neurone. Les dendrites présentent à leurs extrémités des épaississements membranaires, appelés épines dendritiques, où sont détectés les signaux synaptiques provenant d’autres neurones qui permettront ou non la formation du potentiel gradué (cf. suite du cours). Les dendrites contiennent des ribosomes libres leurs permettant de synthétiser certaines de leurs protéines.
- L’axone : est un prolongement unique, fin, homogène, relativement linéaire et pouvant s’arboriser par la suite au niveau des nœuds de Ranvier. Il prend naissance au niveau d’une expansion conique du corps cellulaire appelée cône d’implantation (ou cône d’émergence) qui est également le lieu d’où partira le potentiel d’action (cf. suite du cours). L’axone peut se diviser en une ou plusieurs collatérales qui se termineront généralement par une arborisation terminale dont chaque extrémité, renflée, établit des contacts synaptiques avec les cellules cibles. Les neurones sont principalement constitués de neurofibrilles et de mitochondries qui fournissent l’énergie nécessaire aux mouvements des messagers intracellulaires et à la libération des vésicules synaptiques au niveau des extrémités axonales, appelées boutons synaptiques. L’axone est également le lieu de transports qui sont soit antérograde (vers les boutons synaptique) soit rétrograde (vers le corps cellulaire). Ce transport continuel représente un flux nécessaire à l’apport des différentes macromolécules tout au long de l’axone ; en effet les axones ne présentent aucunes structures responsables de la synthèse de protéines.
b) La gaine de myéline
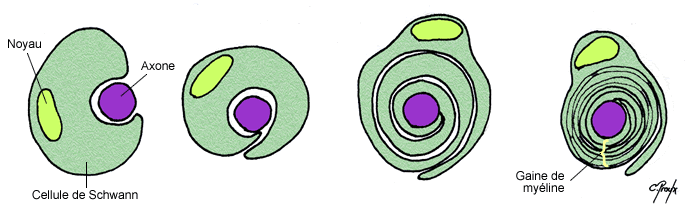
Les axones peuvent être recouverts par une gaine de myéline qui correspond à l’enroulement de couches phospholipidiques concentriques de manière discontinue sur l’ensemble de l’axone. En effet ces gaines sont espacées tous les 1 à 2 mm par les nœuds de Ranvier qui sont du coup amyéliniques et d’où peuvent émerger les collatérales de l’axone. Ces gaines sont formées à partir de 2 types cellulaires suivant si l’on se trouve dans le SNC ou le SNP :
- Dans le SNC on trouve des oligodendrocytes qui envoient des prolongements de leurs corps cellulaires qui recouvreront les axones. Il peut ainsi participer à des gaines de neurones différents.
- Dans le SNP on trouve des cellules de Schwann qui vont s’enrouler entièrement autour d’un axone unique. Leur noyau est renvoyé au niveau de la face la plus externe.
Les gaines isolent électriquement les axones permettant d’accroître la vitesse de transmission des influx nerveux.
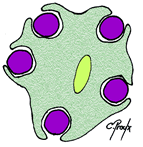
Au niveau du SNP les fibres amyéliniques sont également entourer par des cellules de Schwann mais elles ne s’enroulent pas autour. Ces fibres conduisent lentement l’influx nerveux. Ce sont surtout des fibres du SNV.
Pathologie :
La myéline peut dégénérer par destruction auto-immune, c’est le cas de la sclérose en plaque qui entraîne des troubles de la vue, des problèmes d’équilibre et de coordination, des sensations altérées, des anomalies dans l’articulation des mots, de la fatigue, des incontinences, des troubles sexuels et des troubles cognitifs et affectifs.
c) Classification des neurones
Les neurones peuvent être classés par leurs structures ou par leurs fonctionnalités.
- De manière structurale il existe :
- Les neurones bipolaires (sensitif)
- Les neurones multipolaires (moteur et sensitif)
- Les neurones unipolaires : un prolongement périphérique et un central, tout deux myélinisés (essentiellement sensitif).
- De manière fonctionnelle il existe :
- Les neurones sensoriels
- Les neurones moteurs
- Les inter-neurones, ce sont les plus nombreux et ils servent de lien entre les neurones dans le SNC.
3) Névroglie : cellules gliales et cellules de Schwann
Les cellules de la névroglie sont les cellules majoritaires du système nerveux. Elles sont étroitement liées aux neurones, de taille inférieure à ces derniers et ne forment aucune synapse chimique. Contrairement aux neurones, les cellules gliales peuvent se reproduire par mitose. Elles ont différents rôles au sein des tissus nerveux : l’isolement des tissus nerveux (cf. Oligodendrocytes et cellules de Schwann), les fonctions métaboliques (cf. Astrocytes), le soutien structural et une protection immunitaire (cf. Microglie). La macroglie correspond aux astrocytes et aux oligodendrocytes.
Les cellules gliales, toutes situées dans le SNC, sont de différents types :
- Astrocytes : cellules de petite taille et de forme étoilée, dont leurs extrémités se finissent pas un renflement appelé pied astrocytaire. On distingue deux types d’astrocytes :
- Les astrocytes de type I sont accolés aux capillaires pour en prélever des nutriments comme le glucose et le calcium et pour en déverser le potassium extracellulaire excédentaire. Il y a ainsi un contrôle de l’environnement ionique immédiat des neurones. Ces astrocytes participent, avec les cellules endothéliales, à la formation de la barrière hémato-encéphalique.
- Les astrocytes de type II entourent les neurones et la fente synaptique (recapture du neurotransmetteur).
- Oligodendrocytes : plus petits que les astrocytes. Ils possèdent un cytoplasme plus dense et sont présent dans la substance blanche. Les oligodendrocytes ont comme principale fonction d’envelopper les axones des neurones formant ainsi les gaines de myélines qui donneront la couleur blanche de la substance blanche. Ils peuvent être comparés aux cellules de Schwann du SNP. Un seul oligodendrocyte pourra former plusieurs gaines de myéline sur plusieurs neurones différents (contrairement aux cellules de Schwann).
- Microglie : cellules de petite taille, représentant 5-20% de la population gliale totale. Les cellules microgliales sont présentes en plus grande quantité dans la substance grise que dans la blanche. Elles sont activées suite à une atteinte du SNC puis se déplacent vers les sites atteints où elles se multiplient. Ces cellules appartiennent au groupe des macrophages et phagocytent donc les cellules mortes et les corps étrangers.
- Cellules épendymaires : ce sont des cellules épithéliales (épithélium simple) situées dans certaines cavités de l’encéphale que l’on appelle ventricules. Elles y fabriquent le liquide céphalorachidien qui protège l’encéphale et la moelle épinière tout en participant à satisfaire l’ensemble des besoins physiologiques des cellules du tissu nerveux. Les cellules épendymaires spécialisées qui fabriquent le liquide céphalo-rachidien forment les structures anatomiques appelées les plexus choroïdes. On retrouve aussi ces cellules dans le canal de l’épendyme situé à l’intérieur de la moelle épinière.
II) Transmission de l’influx nerveux et synapses
1) Potentiels et influx nerveux
L’influx nerveux est le potentiel électrique se déplaçant sur l’axone après que le neurone ait été stimulé. L’excitabilité est la capacité à réagir à un stimulus et à le convertir en influx nerveux. La conductivité est la capacité de propagation et de transmission de l’influx nerveux.
La transmission de l’influx nerveux se fait des dendrites jusqu’à l’axone. En effet l’arbre somato-dendritique représente le pôle récepteur du neurone et l’axone (ou collatérales) représente le pôle émetteur du neurone. Attention cela ne veut pas dire que l’axone ne peut pas jouer le rôle de récepteur.
La communication entre neurones se fait grâce :
- aux potentiels d’action conduit au niveau des axones sur de longues distances avec peu de pertes.
- aux potentiels gradués conduit au niveau des dendrites sur de courtes distances avec des pertes importantes.
a) Le potentiel de repos
Les neurones, comme toutes les cellules de l’organisme, sont soumise à une différence de potentiel membranaire (ddp) due aux différences de concentration ioniques de part et d’autre de la membrane. Du côté extracellulaire ce sont surtout les ions Na+ et Cl– qui sont présents, et du côté intracellulaire ce sont surtout les ions K+ et les protéines qui sont présents.
On note que les ions K+ sont ceux qui possèdent la plus grande conductance au sein de la membrane (5 fois plus élevé que les autres ions), il attire donc le potentiel de membrane vers son potentiel d’équilibre (-80 mV) donné par l’équation de Nernst. Le gradient de concentration des ions potassique les pousse à sortir de la cellule, mais l’existence de charge positive dans le milieu extracellulaire créé un gradient électrique de sens contraire au gradient de concentration des ions K+. Autrement dit le potentiel de repos est atteint à l’équilibre, lorsque les forces dues au gradient électrique (qui poussent à faire rentrer les ions K+ dans la cellule) sont égales aux forces dues au gradient de concentration (qui poussent à faire sortir les ions K+ de la cellule).
On arrive à un équilibre des forces, la différence de potentiel est alors de -70 mV. Elle se maintient même si Na+ parvient à rentrer dans la cellule, et ceci par régulation des pompes Na+/K+. On peut faire la remarque que le potentiel de membrane est nul lorsque la concentration en ions chargés négativement est égale à la concentration en ions chargés positivement, et ce dans le milieu intracellulaire et extracellulaire.
Il y a ainsi un léger surplus d’ions chargés positivement dans le milieu extracellulaire et un léger surplus d’ions chargés négativement dans le milieu intracellulaire. Ces excès d’ion s’accumulent contre la membrane (tel un condensateur électrique) et sont à l’origine du potentiel de repos de -70mV qu’il existe entre l’intérieur et l’extérieur de la cellule. Attention, la valeur du potentiel de repos n’est pas toujours de -70mV, sa valeur est caractéristique du type de cellules.
b) Le potentiel gradué
Le potentiel gradué est une inversion locale et de courte durée du potentiel membranaire. Il apparaît au niveau des dendrites et des corps cellulaires et est déclenché par une stimulation extérieure à la cellule (inversion locale de la polarité membranaire). Suite à cette stimulation il y a apparition d’un courant électrique local qui se propageant bilatéralement par rapport au point de stimulation et dont l’intensité diminue avec la distance.
Il est dit gradué, car son voltage est proportionnel à l’intensité de la stimulation. Ce potentiel gradué arrivera jusqu’au corps cellulaire et si son voltage est suffisant il y aura formation d’un potentiel d’action.
c) Le potentiel d’action
Le potentiel d’action est une variation transitoire du potentiel membranaire déclenchée suite à une stimulation, formée au niveau du cône d’émergence et dont la propagation est axonique, unidirectionnelle, avec une intensité qui ne diminue pas avec la distance.
La stimulation peut provenir d’un autre neurone, ou de la stimulation d’un récepteur sensitif qui peut être présent à la surface de l’organisme (peau) ou bien même dans l’organisme lui-même (au niveau des organes). Il peut également y avoir des potentiels d’action auto-entretenu, c’est le cas du cœur (cf. cours physiologie du système cardiovasculaire). Si cette stimulation est suffisante, c’est-à-dire si elle dépasse le seuil de déclenchement du neurone, alors il y aura création du potentiel d’action. Attention le seuil n’est pas le même pour tous les neurones.
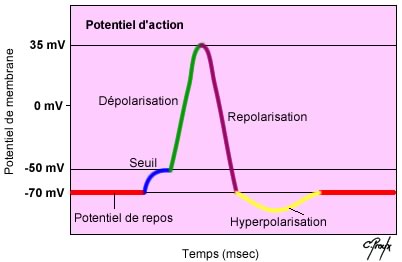
Au niveau des axones on met en évidence une grande concentration de canaux sodique voltage dépendant qui sont responsable de la propagation du potentiel d’action. Le potentiel d’action se fait en différentes étapes :
- La dépolarisation correspond à une augmentation de la perméabilité sodique, qui entraîne une réduction du potentiel membranaire. L’intérieur de la membrane est moins négatif et le potentiel s’approche de 0.
- La repolarisation rapide du point dépolarisé correspond à la fermeture des canaux sodiques et à l’ouverture des canaux potassique plus ou moins décalé dans le temps.
- L’hyperpolarisation correspond à une sortie en excès d’ions K+ lors de la repolarisation ce qui entraîne une augmentation de la différence de potentiel membranaire, plus importante que la différence de potentiel présente au repos. Il y a dès lors intervention des pompes Na+/K+ pour rétablir les concentrations ioniques.
Remarque :
Dans le tissu nerveux toutes les fibres nerveuses sont accolées les unes aux autres, on pourrait alors se poser la question : « Pourquoi l’influx nerveux ne se transmettrait pas de fibres en fibres ? ». La réponse est donnée par le fait que le potentiel d’action ne dure pas assez longtemps pour créer un potentiel d’action sur une autre cellule.
- Si la dépolarisation ne passe pas le seuil (-50mV / -40mV), il n’y aura pas d’influx.
- Si la dépolarisation passe le seuil, la dépolarisation se poursuit jusqu’à + 40mV.
- Quelque soit l’intensité du stimulus, la dépolarisation ne dépasse pas les + 40mV.
Pourtant le SNC peut faire la différence entre un stimulus faible ou fort même si le potentiel d’action est le même et ceci par la capacité de perception de l’intensité du stimulus. En effet plus la force du stimulus augmente plus le nombre de neurones impliqués est grand et la fréquence des potentiels d’actions produits est plus importante si le stimulus est plus fort.
A l’extrémité de l’axone, le signal nerveux passe vers un ou plusieurs neurones qui le transmettent vers d’autres neurones ou des cellules effectrices en franchissant la synapse.
- Pendant la période réfractaire absolue le neurone ne peut dans aucun cas répondre à une nouvelle stimulation. Elle est à prendre en compte jusqu’à ce que le potentiel, lors de la repolarisation, revienne jusqu’au potentiel seuil.
- Pendant la période réfractaire relative le neurone peut répondre à une nouvelle stimulation, mais elle nécessite un stimulus d’autant plus grand qu’on se situe proche de la période réfractaire absolue. Elle prend place tout de suite après la période réfractaire absolue et jusqu’à ce que le potentiel soit de nouveau au niveau du potentiel de membrane de repos.
Les courants locaux qui permettent la propagation de l’influx nerveux sont appelés vagues de dépolarisation/repolarisation.
Dans le cas des neurones amyéliniques, le potentiel d’action possède la même amplitude tout du long ; la dépolarisation en un point induit la dépolarisation du point voisin, la propagation est lente. Il existe une période réfractaire. Le potentiel d’action se déplace en sens unique du cône d’émergence vers les terminaisons.
Dans le cas des neurones myélinisés, il y a création successive des potentiels d’action le long de l’axone ; ceux-ci vont s’éloigner du site d’excitation initiale. La vitesse de transmission dépend du diamètre de la fibre (s’il augmente, la vitesse augmente). La conduction est dite conduction saltatoire (de nœud en nœud) et la propagation est rapide. Après la repolarisation, la membrane demeure inerte un certain temps ; les canaux à Na+ ne peuvent pas s’ouvrir (période réfractaire). Au niveau des nœuds de Ranvier on met en évidence une grande concentration de canaux sodique voltage dépendant qui sont responsable de la propagation du potentiel d’action.
Remarques :
Les invertébrés n’ont pas de neurones myélinisés ; ils doivent donc compenser par leur diamètre (le plus gros axone connu est l’axone géant du réflexe de fuite du calamar ; v=20 m.s-1, diamètre=1mm). Une fibre non myélinisée devrait avoir un calibre de plusieurs centimètres pour conduire l’influx à la même vitesse (100 m/s) qu’une fibre myélinisée de 20 micromètres de diamètre.
2) Synapses et neurotransmissions
La synapse correspond au point de connexion fonctionnel existant entre deux neurones. Un millimètre cube de substance grise du cortex peut contenir 5 millions de synapses. Les synapses peuvent être électriques ou chimiques :
Les synapses électriques correspondent à des jonctions jonction de type GAP (ou nexus) présentent dans de nombreux tissus de l’organisme. Ces synapses sont formées par des protéines transmembranaires qui forment un « tunnel » entre les cellules permettant des échanges (cf. cours de biologie cellulaire).
Les synapses chimiques, quant à elles, sont présentent uniquement dans le tissu nerveux et ce sont elles que nous allons expliquer dans la suite de ce cours. Suivant les cellules impliquées on aura des :
- Synapses neuro-neuronales : jonction entre 2 neurones. Parmi elles on trouve les synapses axo-dendritiques (entre l’axone et les dendrites) et axo-somatiques (entre l’axone et le corps cellulaires).
- Synapses neuro-effectrices : jonction entre un neurone (moteur) et une cellule effectrice (cellule musculaire ou cellule sécrétrice d’une glande, comme la glande surrénale par exemple).
- Synapses sensori-neuronales : jonction entre des cellules sensorielles et des neurones.
Production Mariana RUIZ (LadyofHats) – Traduction Berrucomons
La neurotransmission se fait par libération de vésicules synaptique contenant des neurotransmetteurs au niveau de l’espace synaptique. Ces neurotransmetteurs sont synthétisés par différentes enzymes dans le bouton synaptique ce qui nécessite une grande quantité d’énergie et donc un grand nombre de mitochondries. Le stockage des neuromédiateurs dans des vésicules est nécessaire pour ne pas qu’ils soient dégradés.
Une fois que les neuromédiateurs se sont fixés sur les récepteurs de la membrane post-synaptique, ils doivent être éliminés de la fente synaptique. Cette élimination est soit réalisée par des protéines catalytiques spécifiques (par exemple l’Acétylcholinestérase qui dégrade l’Acétylcholine), soit par réabsorption des neuromédiateurs eux-mêmes par la cellule présynaptique ainsi que par certaines cellules de la névroglie (grâce à des transporteurs spécifiques des neuromédiateurs), soit par diffusion en dehors de la fente synaptique. Des défauts ou excès dans l’élimination des neuromédiateurs de la fente synaptique peut avoir comme conséquence des troubles pathologiques (cf. suite du cours).
- Le neurone présynaptique synthétise les molécules de neurotransmetteurs qui sont stockées dans les vésicules synaptiques au niveau des boutons terminaux.
- L’arrivée de l’influx nerveux (potentiel d’action) au niveau de la terminaison présynaptique provoque la dépolarisation de la terminaison axonale.
- La dépolarisation entraîne l’entrée d’ion calcium (Ca2+) dans la terminaison axonale, grâce à l’ouverture de canaux calcique voltage dépendant présent en grande concentration au niveau des boutons synaptiques.
- Le calcium permet le mécanisme de fusion de la membrane des vésicules synaptiques à la membrane présynaptique.
- Le neurotransmetteur est alors libéré par exocytose dans la fente synaptique. Cette exocytose nécessite de l’énergie fournie par les mitochondries de la terminaison présynaptique.
- Le neurotransmetteur se fixe à ses récepteurs spécifiques localisés sur la membrane post-synaptique.
- Cette fixation entraîne, selon la nature du neurotransmetteur, du récepteur et de la chaîne de transduction, l’ouverture ou la fermeture de canaux ioniques post-synaptique.
- Les variations de conductances ioniques modifient alors la polarisation électrique de cette membrane de façon plus ou moins importante. On parle de potentiel post-synaptique (PPS). La naissance de ce courant post-synaptique modifie le signal électrique du neurone post-synaptique.
- Le neurotransmetteur après action est ensuite inactivé ce qui limite l’existence du PPS. La transmission synaptique est ainsi rendue efficace grâce à l’inactivation rapide des neurotransmetteurs.
Le potentiel post-synaptique peut-être de deux types :
- Il peut être excitateur grâce à l’entrée d’ions sodium Na+, on parle de potentiel post-synaptique excitateur (PPSE). Le PPSE n’est créé que si la dépolarisation dépasse le seuil permettant la formation d’un potentiel d’action et donc la propagation de l’influx nerveux.
- Il peut être inhibiteur, on parle de potentiel post-synaptique inhibiteur (PPSI). Le PPSI est créé par l’entré d’ion chlorure Cl– ou la sortie d’ion potassique K+ qui permettent une hyperpolarisation diminuant l’excitabilité neuronale.
III) Encéphale, moelle épinière et nerfs rachidiens
Comme dit précédemment, le système nerveux central est constitué de l’encéphale et de la moelle épinière.
1) L’encéphale
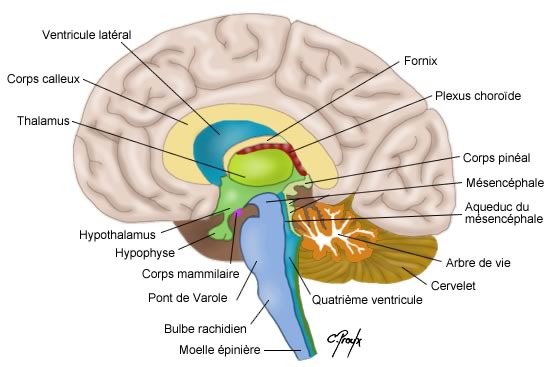
L’encéphale correspond à la partie intra-crânienne du système nerveux centrale. Il comprend :
|
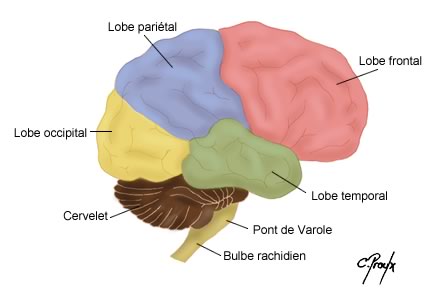
Les hémisphères cérébraux sont divisés anatomiquement par un certain nombre de lobes :
|
On distingue deux grands types de tissus dans le cerveau :
|
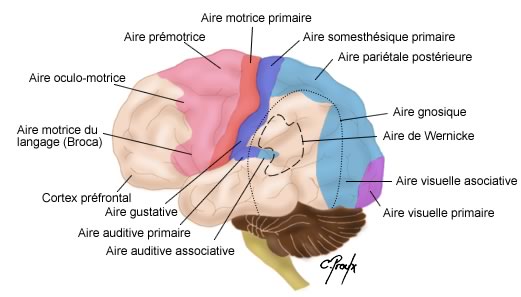
Les neurones présents dans le cerveau sont regroupés suivant leur fonction, de cette manière le cortex peut être divisé en 52 aires fonctionnelles, appelées Aires de Brodmann, que l’on peut diviser en 3 groupes :
|
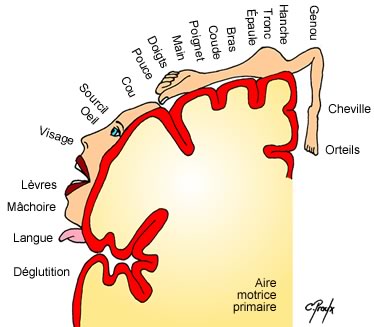
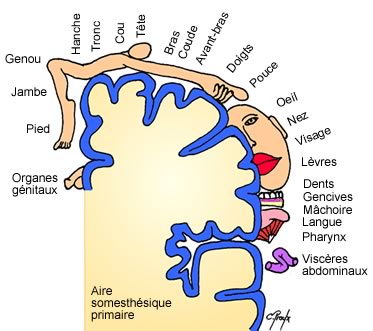
De la même manière que les neurones sont regroupés en aires suivant leur fonction, au sein d’une aire ils sont également regroupés suivant leur zone d’action dans l’organisme. La projection du corps sur les aires permettent d’obtenir des représentations ; on parle d’homonculus moteur pour l’aire motrice primaire et d’homonculus sensitif pour l’aire somesthésique primaire.
Remarques :
La perception sensorielle se fait avec régulation de la motricité du côté opposé. Les deux hémisphères ne sont pas identiques, on parle de latéralisation. Aucune aire fonctionnelle n’est indépendante.
2) La moelle épinière et les nerfs rachidiens
La moelle épinière s’étend du bulbe rachidien à L1 (42cm de long, et 1,8cm d’épaisseur) et se termine par le cône médullaire ou filum terminae. Elle achemine l’influx nerveux provenant et se dirigeant vers l’encéphale et est le centre des réflexes spinaux.
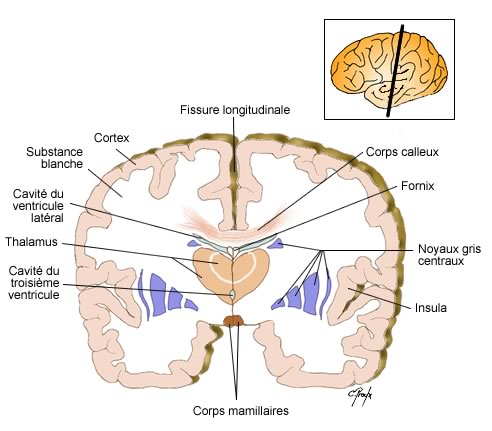
La moelle épinière présente deux renflements : un cervical et un lombaire. Comme l’encéphale, elle est constituée de substance grise (corps cellulaires des neurones) et de substance blanche (neurofibres myélinisées), mais contrairement à l’encéphale, c’est cette fois-ci la substance blanche qui entoure la substance grise. En coupe transversale, la substance grise à la forme d’un papillon. La moelle épinière baigne dans le liquide céphalo-rachidien.
Tout le long, la moelle épinière est le lieu d’émergence des ganglions spinaux.
a) Substance grise et racine des nerfs rachidiens
Tous les neurones de la substance grise de la moelle sont des neurones multipolaires. Au niveau de la moelle thoracique (dorsale) on visualise 3 types de cornes :
- Les cornes postérieures où on trouve les inter-neurones.
- Les cornes antérieures où on trouve les corps cellulaires des neurones moteurs somatiques.
- Les cornes latérales où on trouve les neurones moteurs du SNA (système sympathique) muscles lisses des viscères, muscle cardiaque.
De la moelle sortent deux racines :
- Au niveau des racines rachidiennes antérieures on trouve les axones des neurones moteurs somatiques.
- Au niveau de racines rachidiennes postérieures on trouve les axones des neurones afférents qui véhiculent des influx sensitifs provenant des récepteurs sensoriels périphériques. Les corps cellulaire de ces neurones se trouvent dans les ganglions rachidiens.
Les nerfs rachidiens émergent de chaque côté de la moelle épinière. Issues de l’association des racines antérieures et postérieures.
b) Substance blanche
La substance blanche comprend essentiellement des neurones myélinisés. Les neurofibres sont orientées dans 3 directions :
- Influx sensitif : vers l’encéphale
- Influx moteur : vers le bas de la moelle épinière
- D’un côté à l’autre : de la moelle épinière (neurofibrilles commissurales)
IV) Le réflexe
On distingue deux types de réflexe :
- Le réflexe inconditionné ou inné est une réponse motrice, rapide et prévisible à un stimulus. La conscience n’intervient pas et il est régi par les régions inférieures du SNC (TC et moelle épinière).
- Le réflexe acquis ou conditionné résulte de l’exercice de la répétition.
L’encéphale doit être informé du degré de contraction ou de relâchement de tous les muscles. Le réflexe d’étirement est déclenché par les fuseaux neuromusculaires qui contiennent des cellules musculaires spécialisées ayant la propriété de détecter le degré d’étirement des muscles. Le fuseau neuromusculaire est une entité intramusculaire qui est délimitée par une capsule conjonctive et qui contient plusieurs types de ces cellules musculaires qualifiées de non contractiles (bien qu’elles contiennent tout de même de l’actine et de la myosine en sarcomère) appelées myocyte-intra-fuseau (au nombre de 3 à 10 dans chaque fuseau). Ce fuseau neuromusculaire contient également des terminaisons nerveuses afférentes et efférentes.
- Les fibres afférentes :
- Les terminaisons sensitives primaires ou annulo-spiralées (fibre de type I) correspondent à de grosses neurofibres myélinisées qui entourent les myocyte-intra-fuseau et qui sont stimulées par le degré d’étirement du fuseau. Ces terminaisons vont aller se projeter au niveau d’un motoneurone.
- Les terminaisons sensitives secondaires (fibre de type II) sont également myélinisées et localisées aux extrémités des myocytes-intra-fuseau. Elles sont aussi stimulées par le degré d’étirement du muscle.
- Les terminaisons efférentes :
Les régions contractiles des fuseaux neuromusculaires sont innervées par des neurofibres gamma γ qui assurent la contraction du fuseau. Pour information les neurofibres alpha α assurent la contraction des myocytes extra fuseau.
- Le premier correspond au réflexe monosynaptique. L’étirement du muscle stimule le fuseau neuromusculaire et provoque une augmentation de la fréquence des potentiels d’action dans la neurofibre sensitive de type I. Comme dit précédemment cette neurofibre se projette, dans la moelle épinière, directement au niveau d’un motoneurone α qui entraînera la contraction musculaire des muscles agonistes, les muscles extenseurs.
- Le deuxième correspond au réflexe polysynaptique. Ici c’est un interneurone qui est excité et qui agira au niveau d’un motoneurone, en entraînant cette fois-ci le relâchement des muscles antagonistes.
En même temps que la contraction réflexe, il y a également excitation des neurones moteurs gamma γ. La contraction réflexe du muscle réduit la tension exercée sur le fuseau et provoque une diminution de la fréquence des potentiels d’action.
V) Le système nerveux autonome (SNA)
Le SNA innerve le muscle cardiaque, les muscles lisses et les glandes. Que ça soit le système nerveux sympathique ou parasympathique et sont toujours formés par l’association de deux neurones qui se font synapses dans un ganglion autonome : le premier est pré-ganglionnaire possédant son corps cellulaire dans le SNC et le deuxième est post-ganglionnaire possédant son corps cellulaire dans le ganglion. Les axones des neurones ganglionnaires sont faiblement myélinisés.
Les neurones pré-ganglionnaires libèrent dans les deux cas de l’acétyle-choline afin de transmettre l’influx au deuxième neurone dont le neurotransmetteur sera soit l’acétyle-choline dans le cas du système parasympathique, soit la noradrénaline dans le cas du système sympathique.
L’Ach et la NA peuvent être à la fois excitateurs et inhibiteurs suivant le récepteur touché ; il existe au moins deux types de récepteurs différents pour chaque neurotransmetteur.
- Récepteurs cholinergiques :
- Récepteurs nicotiniques : effet toujours stimulant, au niveau des jonctions neuromusculaires des myocytes squelettiques, de tous les neurones ganglionnaires, et des cellules productrices d’hormones.
- Récepteurs muscariniques : effet inhibiteur ou excitateur selon l’organe cible ; localisés sur tous les organes cibles sympathiques et quelques organes cibles parasympathiques.
- Récepteurs adrénergiques : de type α ou β avec des effets excitateur ou inhibiteur suivant les tissus cibles.
1) Système nerveux sympathique (ou orthosympathique)
Le système nerveux sympathique est caractérisé par le système thoraco-lombaire. Les neurofibres du système orthosympathique prennent naissance au niveau de la moelle dorsale et lombaire (corne latérale de la moelle épinière). Les neurones pré-ganglionnaires du système sympathique sont très court et font synapse dans les ganglions des chaînes latéro-vertébrales. Les neurones post-ganglionnaire sont eux très long et se terminent au niveau des organes.
Le système nerveux sympathique est responsable de toute l’activité inconsciente de l’organisme, telle que le rythme cardiaque, la contraction des muscles lisses, il innerve également la glande médullosurrénale. Le neuromédiateur du système orthosympathique est le NA.
L’activation du système sympathique provoque : mydriase (dilatation de la pupille), tachycardie (augmentation de la fréquence cardiaque), augmentation de la pression artérielle, ralentissement du péristaltisme (mouvements intestinaux), vasoconstriction périphérique (provoquant une pâleur).
2) Système nerveux parasympathique (ou vagal)
Le système nerveux parasympathique est caractérisé par le système crânio-saccral. Les neurofibres émergent de l’encéphale et de la région sacrale de la moelle. Les axones pré-ganglionnaires (très longs) s’étendent du SN aux structures qu’ils innervent. Une fois qu’ils y sont parvenus, ils font synapse avec les neurones ganglionnaires (ganglions terminaux).
Le système parasympathique contrôle les activités involontaires des organes, glandes, vaisseaux sanguins conjointement à l’autre partie du SNA. Il intervient dans certains phénomènes pathologiques, tels les évanouissements de la lipothymie (malaise vagal), diarrhées, vomissement, larmes,… Le neurotransmetteur en jeu est l’acétylcholine, qui sera aussi le neurotransmetteur effecteur au niveau du deuxième neurone.
L’activation du système parasympathique provoque globalement des effets opposés à celles du système sympathique : bradycardie (ralentissement de la fréquence cardiaque ; nerf vague responsable du malaise vagal), baisse de la tension artérielle, augmentation du péristaltisme, myosis (contraction pupillaire), augmentation des sécrétions.