- I) Les intervenants et leurs fonctions
- 1) Les transporteurs d’électrons
- 2) L’ATP synthétase
- 3) L’atténuation physiologique de la douleur
- II) Molécule matriciel & molécule cytosolique
- 1) Les différentes navettes
- a) La navette malate-aspartate
- b) La navette glycérol 3-phosphate
- 2) Bilan énergétique : 36 ou 38 ATP ?
- 1) Les différentes navettes
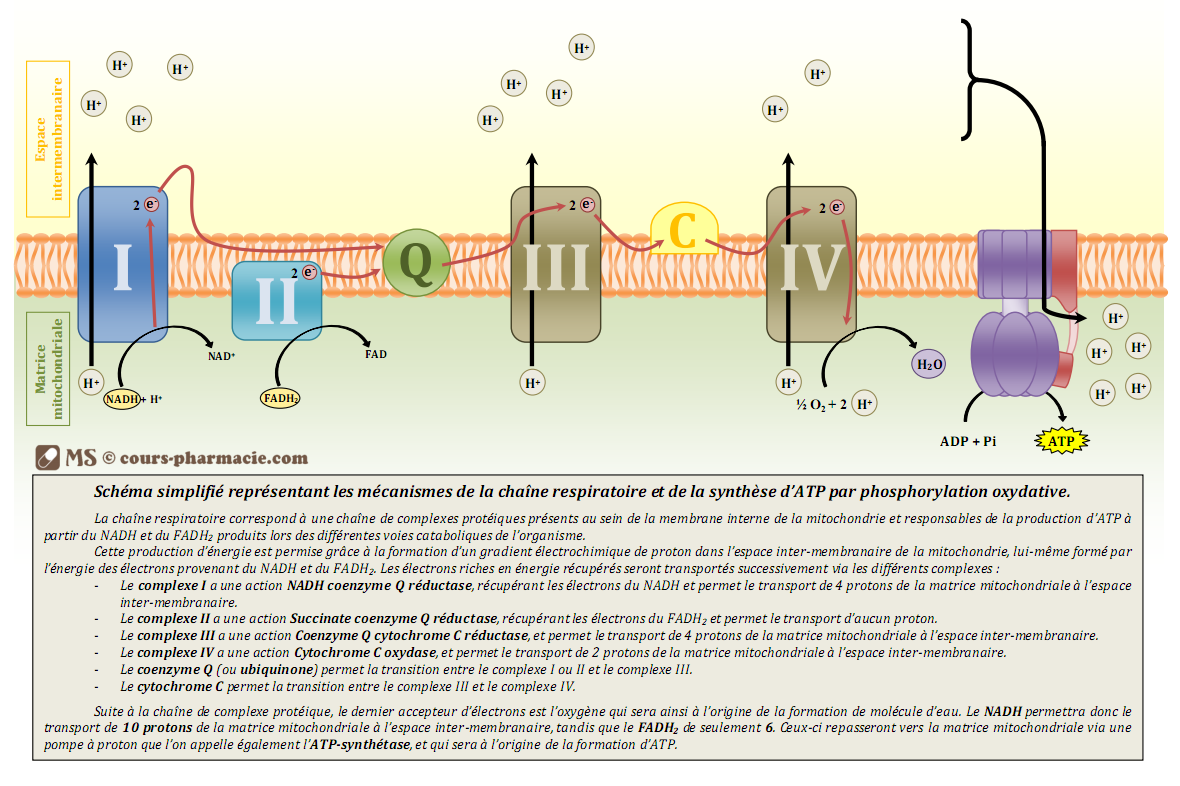
La chaîne respiratoire correspond à une association de complexes protéiques présents au sein de la membrane interne de la mitochondrie et responsable, avec l’ATP synthétase, de la phosphorylation oxydative. Ce processus associe l’oxydation du NADH et du FADH2, tous deux produits lors des différentes voies cataboliques de l’organisme (glycolyse, cycle de Krebs, hélice de Lynen…), à la production d’ATP et ceci grâce à la formation d’un gradient de protons.
I) Les intervenants et leurs fonctions
1) Les transporteurs d’électrons
Tout au long de la chaîne respiratoire les électrons provenant du NADH et du FADH2, vont perdre de l’énergie qui sera utilisée pour former le gradient électrochimique de proton entre l’espace inter-membranaire et la matrice mitochondriale. Les électrons riches en énergie ainsi récupérés seront transportés successivement via les différents complexes :
- Le complexe I a une action NADH coenzyme Q réductase, récupérant les électrons du NADH et permet le transport de 4 protons de la matrice mitochondriale à l’espace inter-membranaire.
- Le complexe II a une action Succinate coenzyme Q réductase, récupérant les électrons du FADH2 et permet le transport d’aucun proton.
- Le complexe III a une action Coenzyme Q cytochrome C réductase, et permet le transport de 4 protons de la matrice mitochondriale à l’espace inter-membranaire.
- Le complexe IV a une action Cytochrome C oxydase, et permet le transport de 2 protons de la matrice mitochondriale à l’espace inter-membranaire.
- Le coenzyme Q (ou ubiquinone) permet la transition entre le complexe I ou II et le complexe III. Il est intéressant de préciser ici que le coenzyme Q accepte également les électrons provenant du cytosol.
- Le cytochrome C permet la transition entre le complexe III et le complexe IV.
Les électrons de basses énergies libérés à la fin de la chaîne respiratoire réagiront ainsi avec les molécules d’oxygène et les protons présents dans la matrice mitochondriale afin de former des molécules d’eau. Le fonctionnement progressif de la chaîne respiratoire est nécessaire car les électrons libérés par le NADH et le FADH2 sont riches en énergie et de cette manière ne peuvent pas réagir d’emblée avec les molécules d’oxygène.
Le NADH permettra donc le transport de 10 protons de la matrice mitochondriale à l’espace inter-membranaire, tandis que le FADH2 de seulement 6.
Le cyanure bloque le transfert d’électrons au niveau du complexe IV par combinaison avec le fer ferrique Fe3+. La roténone est un inhibiteur du complexe I.
2) L’ATP synthétase
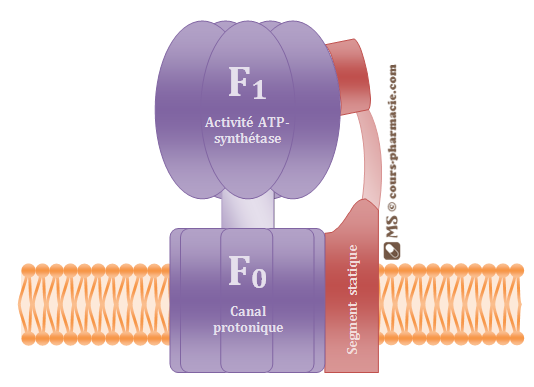
L’ATP synthétase est une pompe ionique inversée, qui au lieu de transporter les protons dans le sens inverse du gradient de concentration, entraîne la synthèse d’ATP grâce au passage des protons dans le sens du gradient.
Elle est constituée d’une sous-unité F0 intra-membranaire qui joue de rôle de canal protonique, d’une sous-unité F1 baignant dans la matrice mitochondriale et qui possède une activité ATP-synthétase, et d’une partie statique stabilisant la structure.
De cette manière le gradient de proton formé de part et d’autre la membrane interne de la mitochondrie permet la synthèse d’ATP qui sera libéré dans la matrice mitochondriale. Les 10 protons du NADH permettront une synthèse théorique de 3 ATP et les 6 protons du FADH2 de 2 ATP.
II) Molécule matriciel & molécule cytosolique
Il est important de faire la distinction entre le rendement de la production d’ATP entre des molécules riches en énergie produites dans la matrice mitochondriale (cycle de Krebs et hélice de Lynen) et celles produites dans le cytosol (glycolyse). En effet les molécules produites dans la matrice interagissent directement avec les complexes protéiques de la chaîne respiratoire, alors que celles produites dans le cytosol devront tout d’abord passer dans la matrice via des navettes.
1) Les différentes navettes
Les molécules de NADH produites dans le cytosol passent facilement à travers la membrane externe de la mitochondrie qui est très perméable. Ceci n’est pas le cas de la membrane interne, obligeant le NADH à transmettre ses électrons riches en énergie à d’autre de molécules de transfert, différentes selon la navette.
a) La navette malate-aspartate
Les électrons riches en énergie sont ici transférés à l’oxaloacétate pour former le malate qui passera dans la matrice mitochondriale où il retransmettra ses électrons au NAD+ afin de reformer le NADH.
La production d’ATP sera donc ici la même que pour les molécules de NADH produites dans la matrice. Cette navette est plus particulièrement présente au niveau du cœur et du foie.
b) La navette glycérol 3-phosphate
Les électrons riches en énergie sont ici transférés au glycérol 3-phosphate qui retransmettra ses électrons au FADH2.
La production d’ATP sera donc ici inférieure aux molécules de NADH produites dans la matrice. Cette navette est plus particulièrement présente au niveau des muscles squelettiques et du cerveau.
2) Bilan énergétique : 36 ou 38 ATP ?
Le but ici est de comprendre pourquoi le bilan énergétique du catabolisme d’une molécule de glucose est tantôt de 36 ATP et tantôt de 38 ATP.
Connaissant maintenant la présence et le fonctionnement des navettes, ainsi que la présence de l’une ou l’autre d’entre elles dans les différents tissus considérés, nous pouvons facilement comprendre cette différence de 2 ATP.
En effet nous somme face à deux situations :
- La première consiste à considérer la navette malade-aspartate qui participe à la production de 3 ATP par molécules de NADH produites au niveau de la glycolyse.
- La deuxième consiste à considérer la navette glycérol 3-phosphate qui permet la production de seulement 2 ATP par molécules de NADH produites au niveau de la glycolyse.